column
「獣医学つれづれ草」 第6話 子牛の難治性下痢症の新たな治療法 便移植療法の有効性 田村 豊 先生
子牛の難治性下痢症の新たな治療法
便移植療法の有効性
酪農学園大学名誉教授 田村 豊
ヒトや動物の腸管内には数百種類の細菌が生息し、それらが免疫や栄養素の分解など我われが生きていくために必要な機能に深く関わっています。これらの細菌集団を腸内フローラと呼び、腸管粘膜に細菌の花が咲き乱れる百花繚乱の様相を呈しているのです。学会などでは常在微生物叢を総称してマイクロビオータ(microbiota)と呼ぶことが増えています。この腸内フローラは食物の栄養分の一部を利用して生活し、腸内細菌間で菌数のバランスを保ちながら生態系を形成しています。最近、わが国の指定難病である潰瘍性大腸炎やクローン病などの医薬品による治療が困難である消化管疾患に腸内フローラそのものを利用しようとする試みがなされています。腸内フローラを構成する微生物をすべて培養することが困難であるとともに、どのような微生物の組合せがそれぞれの疾患に有効であるのかも不明であるため、現時点で分離菌を混合して医薬品として使用することはできません。そこで考えられたのが健康なヒトの糞便を患者に移植するという大胆な治療法です。これを便微生物移植(FMT;fecal microbiota transplantation)あるいは便移植療法と呼ばれています。現在、慶應義塾大学病院や順天堂大学病院などで治療法としてFMTが実施され、ヒトの腸内に生息するClostridioides difficileの異常増殖により起こる腸炎や潰瘍性大腸炎、クローン病などに有効性が認められています。そこで今回は、動物分野におけるFMTの現状について、特に子牛の難治性下痢症への応用研究について紹介したいと思います。
子牛の下痢は最も一般的に見られる疾病であり、育成に影響を及ぼすのみならず時に死に至るなど農場経営を進める上での重大な問題の一つです。原因はさまざまで食餌性の下痢のほか、病原微生物が関与するものも認められます。病原微生物としては、腸管出血性大腸菌やサルモネラなどによる細菌性下痢症や、ロタウイルスやコロナウイルスなどによるウイルス性下痢症、それにコクシジウムやクリプトスポリジウムなどによる寄生虫性下痢症など多彩であることが知られています。この子牛の難治性下痢症に関してFMTを応用し有用性を示した韓国の研究グループからの報告が2020年にNature Communicationsに公表されています1)。非常に権威ある科学誌に掲載されたことからも、この研究の重要性が推し量られます。使用した子牛は中等度から重度の下痢を患っており、Bristol stool scale(BSS)が6~7点を示していました。ここでいうBSSとは、1997年に英国ブリストル大学のHeaton博士が提唱した大便の形状と硬さで7段階に分類する指標です(https://www.med.oita-u.ac.jp/oitaNST/siryo/bristol.pdf)。1~2点は腸内の滞留時間が長く便秘と診断されます。3~5点は正常便で特に4点が理想的です。6~7点は柔らかすぎて下痢と判断されます。この子牛を3群に振り分けて、FMT群20頭(FMT)、対照群として生理食塩水を投与した14頭(CON)、また抗菌薬を投与した23頭(ABX)としました。FMT群には健康な子牛の糞便5頭を混合して5g(50ml,0.1mg/ml)を胃内に0,12,24時間、8日と48日後の5回投与しました。ABX群では、同時点でネオマイシンを経口投与しました。また、下痢が再発した場合はアプラマイシン、スルファジアジン、トリメトプリム、エンロフロキサシンを筋肉内注射しました。
図1に試験開始後の糞便性状を示しました。CONおよびABX群では試験期間中に下痢便を呈していたのに、FMT群が投与2日目からほぼ正常便に近づいていることを示しています。また、治療後の死亡率と完全寛解率を見ると、CON群では14.3%と35.7%だったのが、FMT群では0%と95.0%と劇的な効果を示しています(表1)。一方、ABX群では17.4%と26.1%とCON群とほぼ変わらず通常の抗菌薬治療では回復しないようです。ではなぜFMTを行うことにより下痢子牛の糞便性状を正常化させ、死亡率を低下させたのでしょうか?論文ではFMT群の腸内フローラの構成とメタボローム解析により詳細に検討されています。ここではあまりに専門的になるため概要だけを説明すると、腸内細菌の一種であるPorphyromonadaceae科細菌の上昇と、糞便中のアミノ酸濃度が減少したことが観察されました。つまり、腸内フローラを正常化したと言えるでしょう。また、単に下痢が治癒したのみならず、驚くことにFMT実施後の体重や枝肉重量の増加も観察されています(図2)。6か月齢では有意な変化が観察されませんでしたが、12か月齢と24か月齢では雌雄に係わらずCON群とABX群に比べて有意の体重増加が観察され、枝肉重量(dressed weight)も同様な傾向が認められました。以上のようにFMTは畜産経営にとって非常に有用な方法であることは理解できましたが、問題は再現性と安全性にあると思います。これらを得るためには糞便を提供する牛とFMTを実施する牛の選別が非常に重要と考えられます。特に糞便提供牛の受入れ基準と除外基準は重要と考えられますので、論文から引用すると表2のようになります。糞便提供牛の基準はいろいろと考えられているものの、未知の病原体の混入など安全性に不安が残るものです。そのことを回避するため、ヒトの場合は20歳以上の2親等以内の健康な親族・配偶者、または患者本人より直接指定のあった健康な知人の糞便を使用し、事前に各種のスクリーニング検査を実施しているようです。なお、子牛の難治性下痢症でのFMTの応用に関しては、NOSAI千葉と東北大学との共同研究で実施されているようです2,3)。
以上のように子牛の難治性下痢症に対するFMTの有効性を紹介しました。では他の家畜でのFMTの応用状況はどのようなものでしょうか?病気の治療ではないのですが、健康な鶏の糞便をヒナに経口投与してSalmonella属菌の侵入を防止するとの研究が1973年になされています4)。これは健康な鶏の盲腸内容物、あるいはその培養物をヒナに経口投与して、腸内フローラを早期に形成させSalmonella属菌の腸管への定着を競合排除する方法です。この方法はCE(competitive exclusion)法あるいは開発者に因んでヌルミ法と呼ばれています。現在、サルモネラの防除には衛生管理の充実や、ワクチン接種、CE法の利用などの総合的な防除法で行っています。この結果、諸外国ではサルモネラ食中毒は増加傾向にあるものの、日本は減少傾向にあるのです。また、病気の治療までは確立されなかったのですが、豚に対するFMTによる腸内での細菌定着パターンと宿主応答の応用研究もなされています5)。現在、世界的に家畜における抗菌薬の過剰使用や誤用により薬剤耐性菌が出現・増加し、畜産物を介してヒトに伝播することによる健康上の問題点が指摘されています。そのため家畜に使用する治療用の抗菌薬は慎重に使用することが求められていますし、成長促進目的での抗菌性飼料添加物は徐々に中止される方向にあります。もし仮に子牛の難治性下痢症に対してFMTが実用化されると、治療効果や成長促進効果も期待でき、抗菌薬の使用を抑制することになり、非常に重要な薬剤耐性菌対策になることが期待されます。この点からも今後の研究の進展を楽しみにしたいと思います。
1)KimHS, Whon TW, Sung H,et al. : Longitudinal evaluation of fecal microbiota transplantation for ameliorating calf diarrhea and improving growth performance. Nature Communications (2021) 12:161 | https://doi.org/10.1038/s41467-020-20389-5 | www.nature.com/naturecommunications
2)田中秀和,大谷夏輝,菊池充人ほか:難治性下痢子牛に対する糞便微生物移植(Fecal Microbiota Transplantation: FMT)の有効性の検討.家畜感染症学会誌 9:93-103, 2020.
3)石井優江,大谷夏輝,清水優ほか:子牛の難治性下痢症に対する糞便微生物移植(FMT)の効果と検証.家畜診療 693:150, 2021.
4)Nulmi E and Rantala M: New aspects of Salmonella infection in broiler production. Nature 241:210-211, 1973.
5)Brunse A, Martin L, Rasmussen TS, et al.: Effect of fecal microbiota transplantation route of administration on gut colonization and host response in preterm pigs. ISME J. 13, 720–733 (2019).
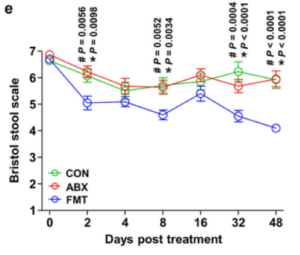
図1.糞便性状の経過


図2.試験群の体重と枝肉重量
